L’équipe CARE (Cancer, Aging, Radiobiology & Environment) développe des projets centrés autour de 3 grands axes : environnement, cancer et vieillissement, avec des spécificités liées à sa tutelle CEA via son implication dans des thématiques telles que la radiobiologie et la toxicologie nucléaire ou les technologies pour la santé (nanoparticules).
Dans l’axe environnement, l’équipe développe des modèles 3D permettant d’analyser les conséquences d’une exposition à de faibles doses de radionucléides (uranium naturel). Elle s’intéresse également aux stratégies de décontamination/décorporation visant à protéger les populations contre les effets de différents radionucléides (uranium, iode).
Dans l’axe cancer, l’équipe a pour but de générer des nanoparticules pour cibler la niche prémétastatique osseuse et accroître la radiosensibilité des tumeurs.
En ce qui concerne l’axe vieillissement, l’équipe étudie spécifiquement le vieillissement osseux en préclinique via l’analyse d’un modèle de vieillissement osseux accéléré et via des études cliniques avec le service de Rhumatologie du CHU de Nice.
Dans ces 3 axes, l’analyse du rôle de l’autophagie est une thématique transversale.
MOTS CLES
Cellules osseuses
Autophagie
Vieillissement
Ostéoporose
Syndrome de Rothmund-Thompson
Ostéosarcome
Métastases osseuses
Microenvironnement
Nanoparticules
Uranium naturel
Iode
Capteurs RFID implantables
E-santé préclinique
AXES DE RECHERCHE
- Axe Cancer
-
PLBio Le projet vise à générer un inducteur d’autophagie à tropisme osseux afin d’analyser l’effet préventif et/ou curatif sur le développement de tumeurs osseuses (ostéosarcome & métastases osseuses).
Logos PLBio
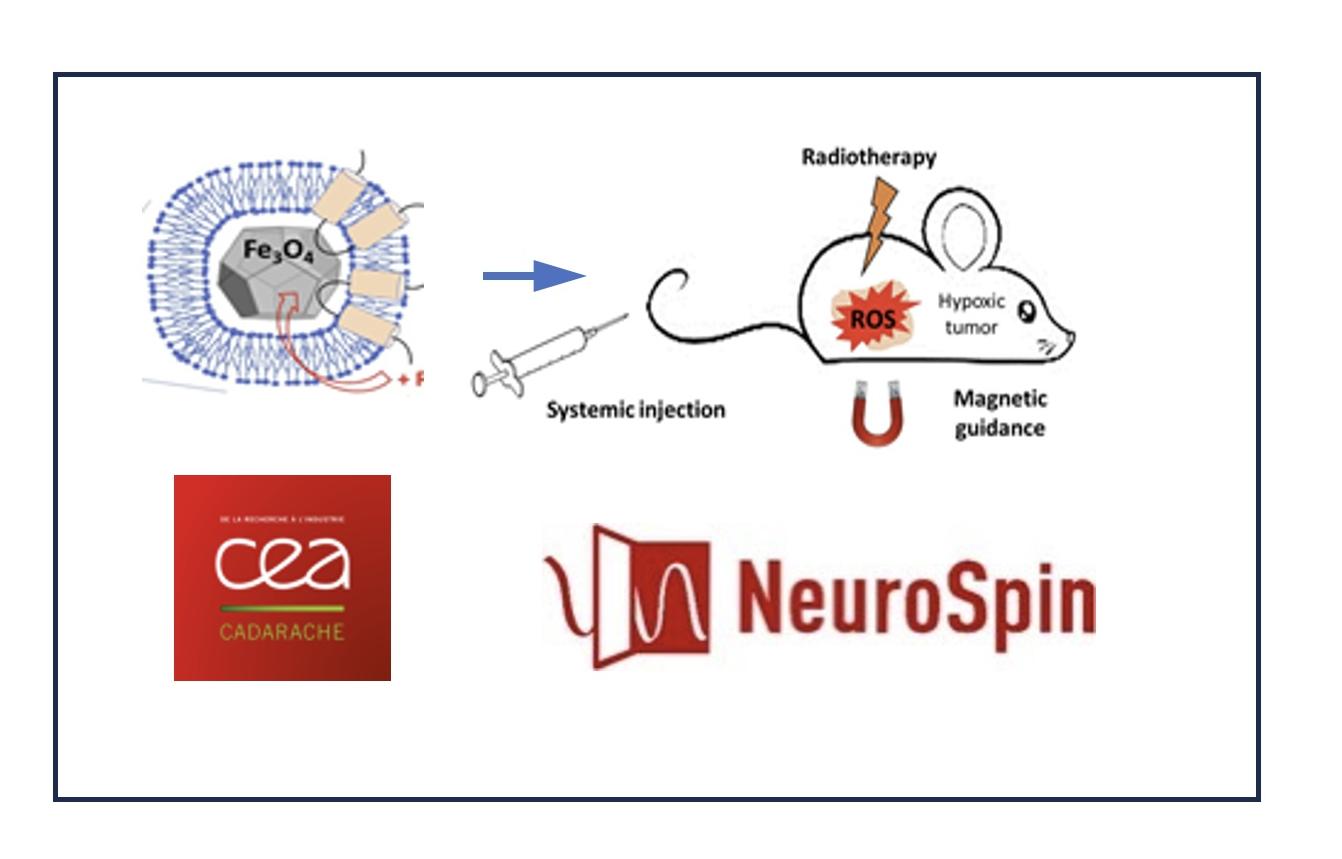
PCSI L'objectif du projet RadioMagnet est de générer des outils magnétotactiques innovants par leur capacité accrue de pénétration dans les tissus et leur pouvoir tumoricide en combinaison aux radiations. Logos PCSI Nanoparticules pour le traitement du cancer
Dans cet axe, nous développons des nanoparticules pour le ciblage de la niche prémétastatique osseuse ainsi que des nanoparticules pour radiosensibiliser des tumeurs via des approches innovantes.
- Rôle de l’autophagie dans la création de la niche prémétastatique osseuse. L'os est un site attractif pour la colonisation tumorale, non seulement pour les tumeurs primitives (ostéosarcome), mais surtout pour les métastases de différents cancers (sein, prostate, poumon, …). Nos résultats ont permis de montrer qu’un microenvironnement osseux déficient en autophagie (inactivation du gène Atg5) stimule le développement tumoral de l'ostéosarcome et des métastases osseuses de cancer du sein. L’analyse des mécanismes impliqués suggère que la diminution de l’autophagie pourrait faciliter la création de la niche prémétastatique osseuse. Les objectifs du projet sont de générer un inducteur d'autophagie à tropisme osseux sous forme de nanoparticules afin d’analyser son impact sur le développement tumoral. Ce projet est lauréat d’un appel d’offre PLbio de l’INCa (coordination V. Pierrefite-Carle Equipe CARE, 2024-2028, collaboration UMR 6286 CNRS, Nantes Université et ICN UniCA).
logos VPC
- Approche innovante en radiosensibilisation. Notre équipe a travaillé depuis plusieurs années avec des nanoparticules de nature métallique et d’origine synthétique ou biogénique, afin d’optimiser différentes modalités de radiothérapie (RT), telle que la radiothérapie à l’I131 dans le cas du cancer thyroidien ou encore les radiothérapies externes comme la RT conventionnelle et la protonthérapie. Ce projet vise à évaluer le potentiel thérapeutique des bactéries magnétotactiques (MTB) génétiquement modifiées produisant des “ROS-enhancer” (nanoparticules biogéniques) en combinaison à une irradiation sur des modèles tumoraux. Ce projet, réalisé par B. Cambien, est lauréat d’un appel d’offre PCSI de l’INSERM (2023-2026, collaboration Neurospin et CEA Cadarache). - Axe Vieillissement
-
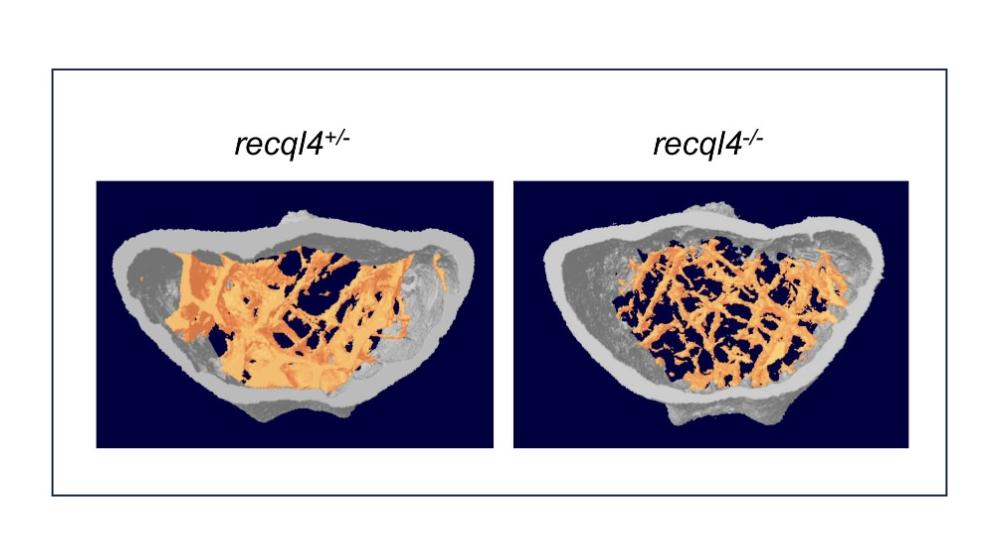
RecQ Des reconstructions 3D d’images de micro-scanner représentatives de fémurs distaux de souris mâles Recql4+/- et Recql4-/- de 13 mois montrent une perte osseuse chez les souris mutantes.
SFR
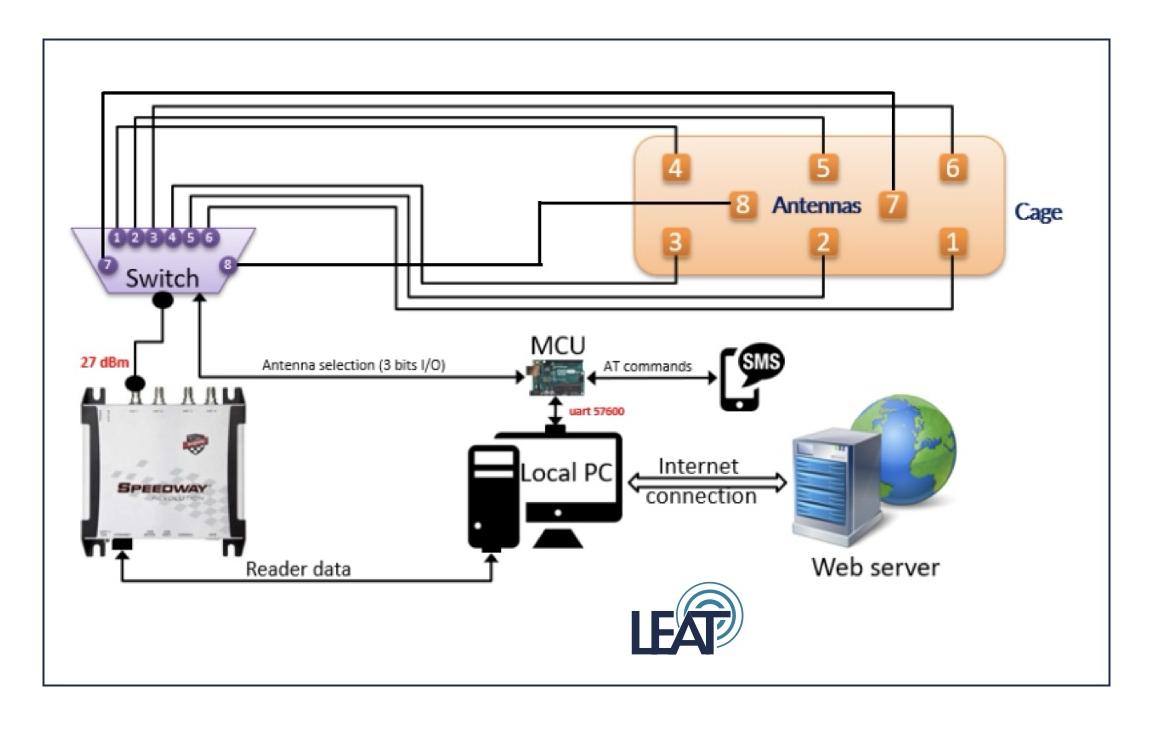
E-santé Ce système d'antennes permet une surveillance H24/J7 appliquée dans des protocoles expérimentaux de vieillissement Logo e-santé Vieillissement pathologique
- Vieillissement osseux. Nous étudions le vieillissement osseux à l’aide d’un modèle murin imitant le syndrome de Rothmund-Thomson de type II, une maladie génétique rare due à des mutations dans le gène de l’hélicase RECQL4. Nous avons montré que les souris Recql4-/- présentent un vieillissement osseux prématuré et une matrice extracellulaire osseuse altérée. Nous voulons poursuivre nos travaux afin d’identifier les mécanismes moléculaires dépendants de l’hélicase RECQL4 impliqués dans la modification de la matrice et analyser comment ces modifications favorisent la perte osseuse. Ce projet, réalisé par S. Santucci-Darmanin a préalablement obtenu des financements de la Société française de Rhumatologie.
Logo
- E-santé préclinique. Nous avons développé un système permettant de traiter et transmettre en temps réel les informations de localisation de rongeurs au sein d’une cage d’hébergement standard. Ce type de données traduisant le comportement, et par extension l’état sanitaire des animaux, va permettre une surveillance H24/J7 appliquée dans des protocoles expérimentaux de vieillissement, mais aussi de suivi de différentes pathologies (maladies neurodégénératives, cancers, atteintes osseuses,…). Ce projet, réalisé par G. Carle fait l’objet d’un brevet international (WO 2020/193252 A1) et d’un projet de pré-maturation engagé avec CNRS-INNOVATION et un groupe industriel international (collaboration LEAT – UMR7248 CNRS-UniCA). - Axe environnement
-
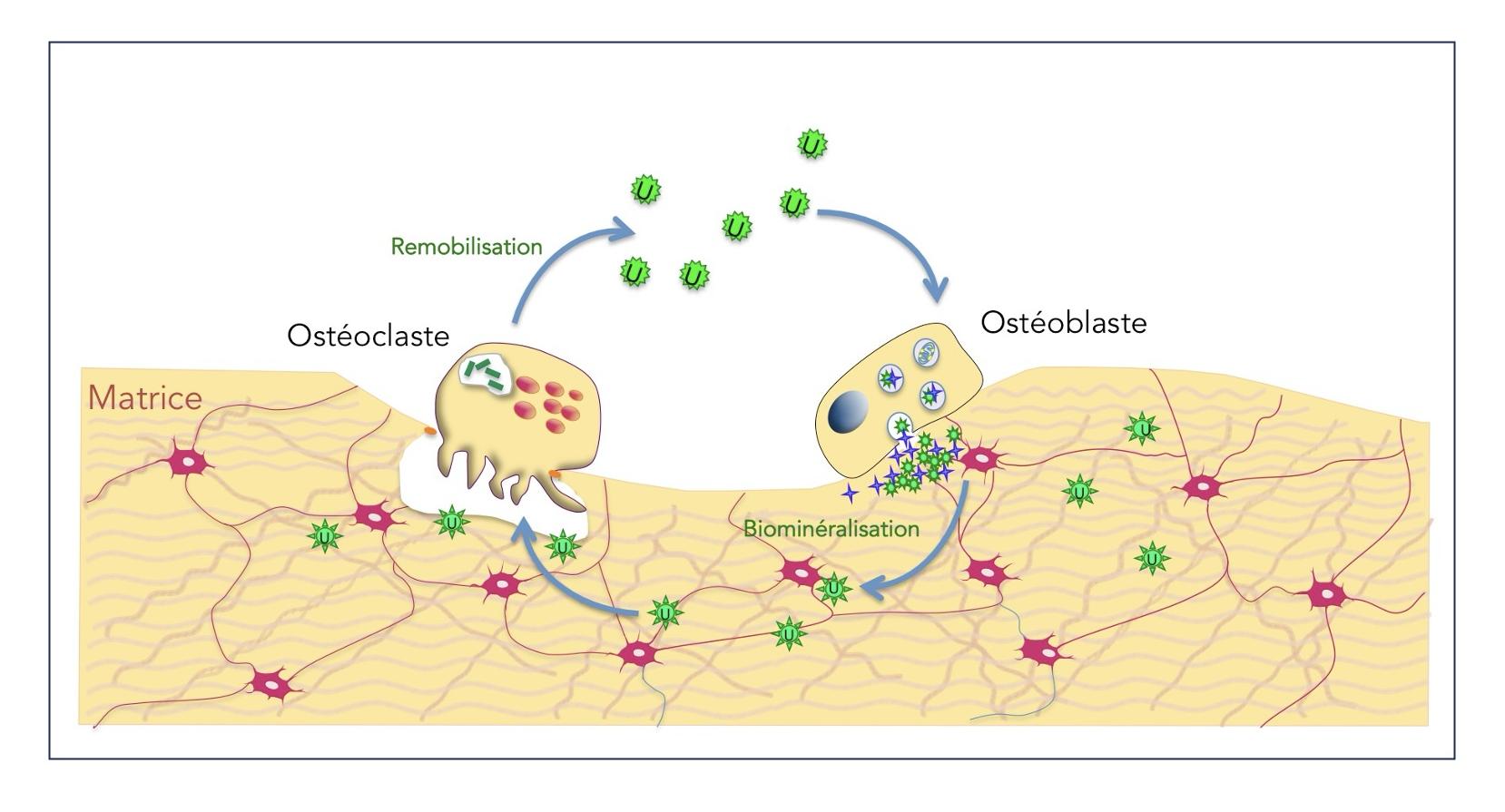
Cycle U L'uranium naturel est biominéralisé par les ostéoblastes puis remobilisé via la résorption par les ostéoclastes
Logo ANR
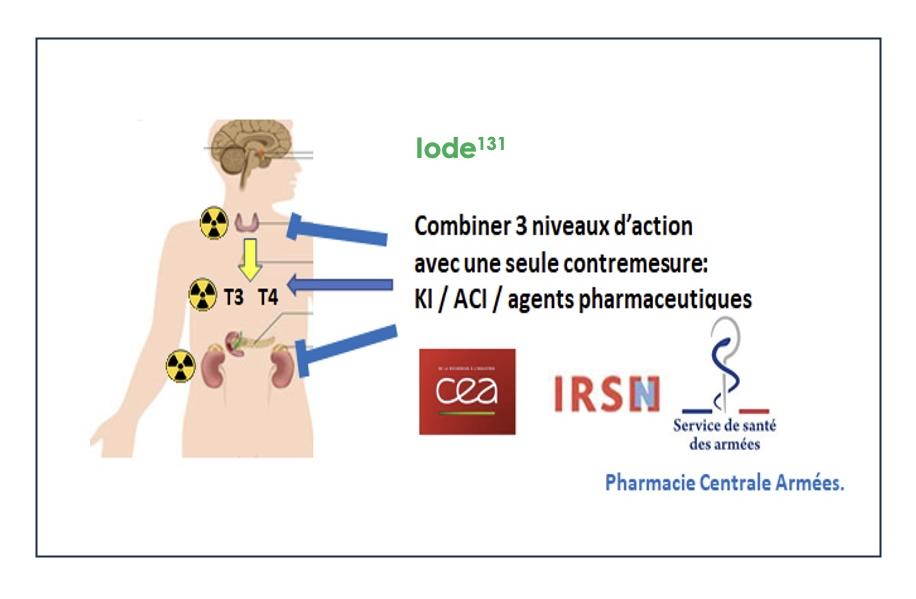
ProDir L’objectif du projet ProDIR est de tester sur des modèles précliniques des combinaisons de contre-mesures permettant d’agir au niveau de tous les organes cibles contaminés par l'131I et impliqués dans sa re-circulation: la thyroïde, les glandes salivaires, l’estomac et la réabsorption rénale.
Logo ANR Exposition environnementale ou accidentelle aux radionucléides
La crise climatique et le contexte géopolitique international ont remis sur le devant de la scène les préoccupations liées au nucléaire. Une meilleure compréhension des mécanismes sous-jacents à la toxicité des radionucléides est cruciale pour l’évolution des normes de protection, l’élaboration des méthodes de remédiation/décorporation et pour la mise en place de systèmes de gestion des risques.
L’équipe CARE développe deux projets dans cette thématique :
- Analyse des mécanismes cellulaires et moléculaires impactés par l’uranium (U) naturel à faibles doses dans le tissu osseux, qui représente le principal site de stockage à long terme. Nous analyserons la distribution et les cibles moléculaires de l’U dans les cellules osseuses ainsi que les voies cellulaires impactées, en particulier l’autophagie et l’inflammation. Ce projet permet également le développement de systèmes osseux biomimétiques 3D qui représentent des outils puissants pour l'évaluation d'agents potentiels de décorporation de l'U. Ce projet qui avait été lauréat d’une 1ère ANR (coordination G. Carle 2016-2021), est lauréat d’une seconde ANR (coordination S. Santucci-Darmanin Equipe CARE, 2023-2027, collaboration ICN UniCA, IRSN, ISA Université de Lyon).
- Radioprotection de la thyroïde & la décontamination des populations exposées à l’iode I131. Suite à l'accident de Tchernobyl, 5 000 cancers de la thyroïde ont été diagnostiqués, principalement chez des personnes qui étaient enfants au moment de l'exposition. Identifier des méthodes de décontamination reste donc une priorité. Le projet vise à analyser les effets d’une contre-mesure basée sur l’administration de pastilles d’iode, d’agents de contraste iodés et de différents agents pharmaceutiques permettant de combiner différents niveaux d’action pour l’élimination de ce radionucléïde. Ce projet est lauréat d’une ANR (coordination B. Cambien Equipe CARE, 2026-2029, collaboration IRSN & Pharmacie centrale des armées.
- Zone d'imagerie isotopique micro-SPECT-CT
-
SPECT Caméra micro-SPECT-CT Iode detection
Cette zone est dotée de plusieurs zones “surveillées”, à savoir, une zone d’imagerie scanner et isotopique et une zone d’hébergement.
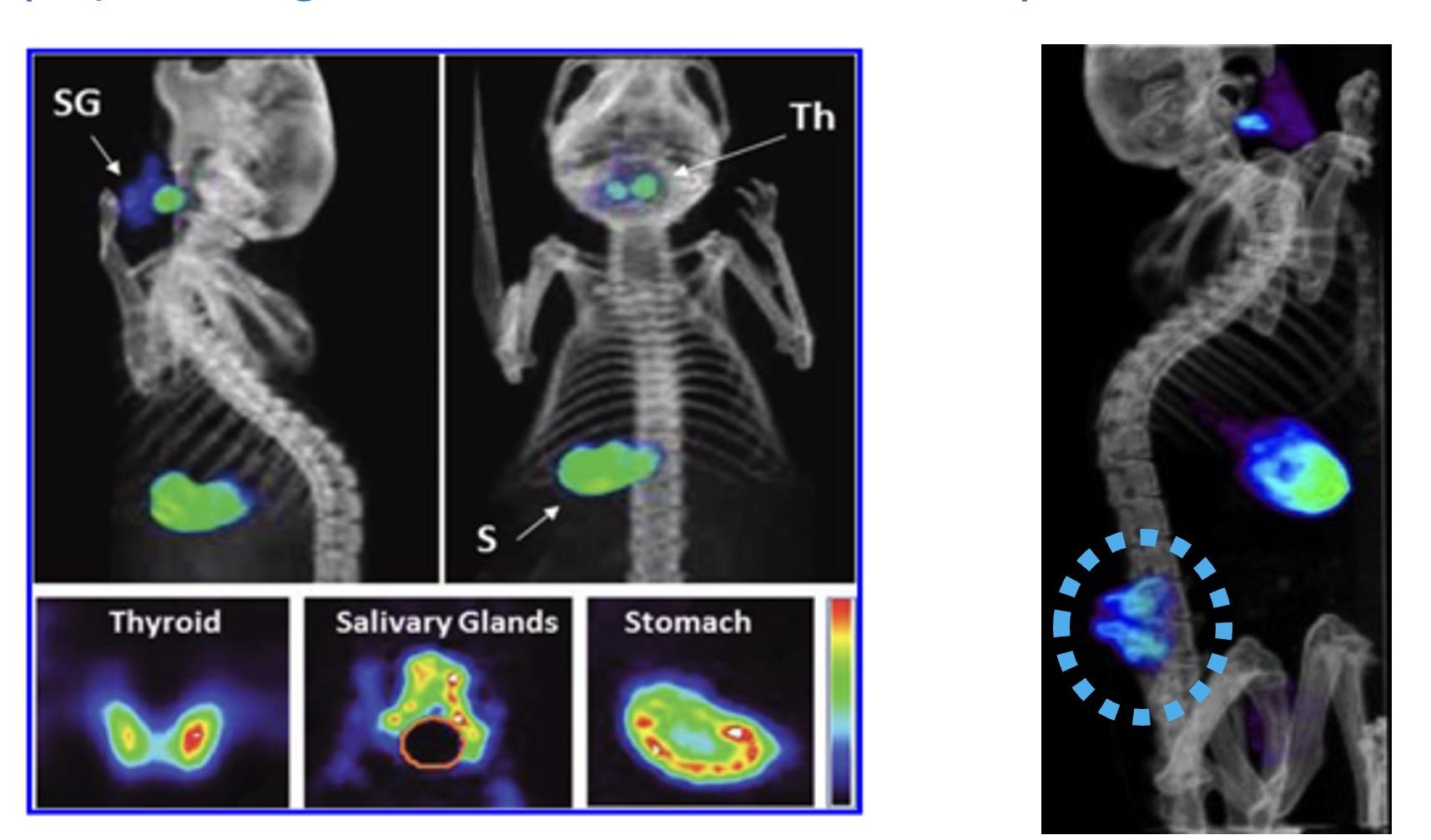
Le détecteur gamma (SPECT) permet le détection d'organes capteurs d'iode (thyroïde, glandes salivaires, estomac) et de tumeurs.
Le scanner X permet des radiographies osseuses et la détection de la fibrose pulmonaire.
- Membres de l'équipe
-
- Valérie PIERREFITE-CARLE, CRHC INSERM, co-responsable équipe
- Béatrice CAMBIEN, CR INSERM, co-responsable équipe
- Georges CARLE, DR1 CNRS
- Sabine SANTUCCI-DARMANIN, CR CNRS, co-Dir PHEN-X
- Véronique BREUIL, PU-PH Rhumatologie, DU PHEN-X
- Olivier CAMUZARD, PU-PH Chirurgie réparatrice
- Marie-Charlotte TROJANI, Post-doctorante SFR
- Tatiana GRITSAENKO, IR ANR UniCA
- Clémence FINET, doctorante (co-dir IRSN)
- Nayara JAROWYS, TR UniCA
- Christophe WILEMSKI, AJT UniCA
- Gaëlle PINI, IR UniCA
- Romane MONTESI, AI CDD PCSI
- Publications
-
Simoneau B, Hurault L, Carle GF, Pierrefite-Carle V, Santucci-Darmanin S. A new in vitro uranium sequestration assay to analyze the effectiveness of 3,4,3-LI(1,2-HOPO) in reducing the harmful effects of this actinide on bone cells. Environ Toxicol Pharmacol. 2024 Sep;110:104518.
Trojani MC, Santucci-Darmanin S, Breuil V, Carle GF, Pierrefite-Carle V. Lysosomal exocytosis: From cell protection to protumoral functions. Cancer Lett. 2024 Aug 10;597:217024.
Trojani MC, Clavé A, Bereder I, Camuzard O, Bernard De Dompsure R, Gonzalez JF, Trojani C, Santucci-Darmanin S, Carle GF, Breuil V, Pierrefite-Carle V. Autophagy markers are decreased in bone of osteoporotic patients: a monocentric comparative study. Eur J Endocrinol. 2024 Mar 2;190(3):K27-K31.
Camuzard O, Nollet M, Santucci-Darmanin S, Trojani, MC, Ben Abderrahman N, Virolle V, Burel-Vandenbos F, Pagnotta S, Orange F, Kolano-Merlin E, Carle GF, Pierrefite-Carle V. Autophagy inactivation in osteosarcoma leads to the appearance of poor prognosis-associated factors. Autophagy Reports, 2022 Sept; 1(1) :418-37.
Gritsaenko T, Pierrefite-Carle V, Creff G, Simoneau B, Hagège A, Farlay D, Pagnotta S, Orange F, Jaurand X, Auwer CD, Carle GF, Santucci-Darmanin S. Low doses of uranium and osteoclastic bone resorption: key reciprocal effects evidenced using new in vitro biomimetic models of bone matrix. Arch Toxicol. 2021 Mar;95(3):1023-1037.
Castillo-Rivera F, Ondo-Méndez A, Guglielmi J, Guigonis JM, Jing L, Lindenthal S, Gonzalez A, López D, Cambien B, Pourcher T. Tumor microenvironment affects exogenous sodium/iodide symporter expression. Transl Oncol. 2021 Jan;14(1):100937.
Cambien B, Lebrigand K, Baeri A, Nottet N, Compin C, Lamit A, Ferraris O, Peyrefitte CN, Magnone V, Henriques J, Zaragosi LE, Giorgetti-Peraldi S, Bost F, Gautier-Isola M, Rezzonico R, Barbry P, Barthel R, Mari B, Vassaux G. Identification of oncolytic vaccinia restriction factors in canine high-grade mammary tumor cells using single-cell transcriptomics. PLoS Pathog. 2020 Oct 19;16(10):e1008660.
Hichri M, Vassaux G, Guigonis JM, Juhel T, Graslin F, Guglielmi J, Pourcher T, Cambien B. Proteomic Analysis of Iodinated Contrast Agent-Induced Perturbation of Thyroid Iodide Uptake. J Clin Med. 2020 Jan 23;9(2):329.
Hafsi M, Preveral S, Hoog C, Hérault J, Perrier GA, Lefèvre CT, Michel H, Pignol D, Doyen J, Pourcher T, Humbert O, Thariat J, Cambien B. RGD-functionalized magnetosomes are efficient tumor radioenhancers for X-rays and protons. Nanomedicine. 2020 Jan;23:102084.
Hafsi M, Preveral S, Hoog C, Hérault J, Perrier GA, Lefèvre CT, Michel H, Pignol D, Doyen J, Pourcher T, Humbert O, Thariat J, Cambien B. RGD-functionalized magnetosomes are efficient tumor radioenhancers for X-rays and protons. Nanomedicine. 2020 Jan;23:102084.
Camuzard O, Trojani MC, Santucci-Darmanin S, Pagnotta S, Breuil V, Carle GF, Pierrefite-Carle V. Autophagy in Osteosarcoma Cancer Stem Cells Is Critical Process which Can Be Targeted by the Antipsychotic Drug Thioridazine. Cancers (Basel). 2020 Dec 7;12(12):3675.
Camuzard O, Santucci-Darmanin S, Carle GF, Pierrefite-Carle V. Autophagy in the crosstalk between tumor and microenvironment. Cancer Lett. 2020 Oct 10;490:143-153.
Hurault L, Creff G, Hagège A, Santucci-Darmanin S, Pagnotta S, Farlay D, Den Auwer C, Pierrefite-Carle V, Carle GF. Uranium Effect on Osteocytic Cells In Vitro. Toxicol Sci. 2019 Jul 1;170(1):199-209.
Renault JP, Carrot G, Pourcher T, Cambien B. Improving 131I Radioiodine Therapy By Hybrid Polymer-Grafted Gold Nanoparticles. Int J Nanomedicine. 2019 Sep 30;14:7933-7946.
Camuzard O, Santucci-Darmanin S, Carle GF, Pierrefite-Carle V. Role of autophagy in osteosarcoma. J Bone Oncol. 2019 Apr 3;16:100235.
Vassaux G, Zwarthoed C, Signetti L, Guglielmi J, Compin C, Guigonis JM, Juhel T, Humbert O, Benisvy D, Pourcher T, Cambien B. Iodinated Contrast Agents Perturb Iodide Uptake by the Thyroid Independently of Free Iodide. J Nucl Med. 2018 Jan;59(1):121-126.
Gritsaenko T, Pierrefite-Carle V, Lorivel T, Breuil V, Carle GF, Santucci-Darmanin S. Natural uranium impairs the differentiation and the resorbing function of osteoclasts. Biochim Biophys Acta Gen Subj. 2017 Apr;1861(4):715-726.
Pierrefite-Carle V, Santucci-Darmanin S, Breuil V, Gritsaenko T, Vidaud C, Creff G, Solari PL, Pagnotta S, Al-Sahlanee R, Auwer CD, Carle GF. Effect of natural uranium on the UMR-106 osteoblastic cell line: impairment of the autophagic process as an underlying mechanism of uranium toxicity. Arch Toxicol. 2017 Apr;91(4):1903-1914.
Camuzard O, Santucci-Darmanin S, Breuil V, Cros C, Gritsaenko T, Pagnotta S, Cailleteau L, Battaglia S, Panaïa-Ferrari P, Heymann D, Carle GF, Pierrefite-Carle V. Sex-specific autophagy modulation in osteoblastic lineage: a critical function to counteract bone loss in female. Oncotarget. 2016 Oct 11;7(41):66416-66428.
Zwarthoed C, Chatti K, Guglielmi J, Hichri M, Compin C, Darcourt J, Vassaux G, Benisvy D, Pourcher T, Cambien B. Single-Photon Emission Computed Tomography for Preclinical Assessment of Thyroid Radioiodide Uptake Following Various Combinations of Preparative Measures. Thyroid. 2016 Nov;26(11):1614-1622.
Pierrefite-Carle V, Santucci-Darmanin S, Breuil V, Camuzard O, Carle GF. Autophagy in bone: Self-eating to stay in balance. Ageing Res Rev. 2015 Nov;24(Pt B):206-17. doi: 10.1016/j.arr.2015.08.004.
Nollet M, Santucci-Darmanin S, Breuil V, Al-Sahlanee R, Cros C, Topi M, Momier D, Samson M, Pagnotta S, Cailleteau L, Battaglia S, Farlay D, Dacquin R, Barois N, Jurdic P, Boivin G, Heymann D, Lafont F, Lu SS, Dempster DW, Carle GF, Pierrefite-Carle V. Autophagy in osteoblasts is involved in mineralization and bone homeostasis. Autophagy. 2014;10(11):1965-77.
- Partenaires
-
logos soutien INCa - Prix et distinctions
-
- Prix SFBMEC - T. Gritsaenko, SFBMEC 2019 Reims
- Prix d'excellence UCA - O. Camuzard, 2019 Nice
- Prix d'excellence UCA - T. Gritsaenko, 2019 Nice
- Prix meilleure communication orale - O. Camuzard, SFBTM 2018 Monaco
- Prix Fondation ARC meilleur poster - O. Camuzard, CFATG 2017 Paris
- Anciens membres
- Bastien SIMONEAU, doctorant 2019-2022
Lucile HURAULT, doctorante 2015-2018
Actuellement Chef de projet R&D Perkin Elmer - Cisbio, Avignon, France
Van Hieu NGUYEN, doctorant 2015-2018 (co-encadrement LEAT, UCA)
Actuellement employé Insight SIP, Sophia Antipolis, France
Philippe PERISSOL, doctorant 2012-2015 (co-encadrement LEAT, UCA)
Actuellement employé F. Iniciativas, Biot, France
Sonia DUARTE, doctorante (co-encadrement University of Coimbra, Portugal)
Actuellement Investigator Center for Neuroscience and Cell Biology, University of Coimbra, Portugal